2025 ESMO | 中国创新药火力全开
2025年欧洲肿瘤内科学会年会(ESMO)已于10月17日至21日在德国柏林顺利落下帷幕。本届大会汇聚了全球肿瘤学领域多项突破性进展,引人瞩目的是,中国共有23项研究入选“突破性摘要”,创下历史新高。在备受关注的主席研讨会环节,三场报告分别公布了针对肺癌、尿路上皮癌等瘤种的关键Ⅲ期临床试验数据,引发学术界广泛讨论。本文将以这三款重磅药物为焦点,回顾中国创新药研发在国际舞台上的高光时刻。
PD-1/VEGF双抗——依沃西依沃西
(AK112)是由康方生物自主研发的全球首创PD-1/VEGF双特异性抗体。10月19日,其注册性III期临床研究——AK112-306(HARMONi-6)的结果在ESMO年会主席论坛上重磅发布,并同步发表于《柳叶刀》杂志。该研究旨在评估依沃西联合化疗对比替雷利珠单抗联合化疗,用于晚期鳞状非小细胞肺癌(sq-NSCLC)一线治疗的疗效与安全性。研究结果显示,依沃西联合化疗mPFS达11.14个月,PFS HR=0.60,P<0.0001;两组间mPFS绝对值差值达4.24个月(△PFS=4.24个月),依沃西联合化疗较替雷利珠联合化疗显著延长患者无进展生存期。
根据Pharma ONE药物研发大数据平台显示,依沃西已在中国获批两项适应症:EGFR-TKI治疗进展的局部晚期或转移性非鳞NSCLC和PD-L1阳性(TPS≥1%)晚期NSCLC,成为全球首个获批上市的“肿瘤免疫+抗血管生成“协同抗肿瘤机制的双特异性抗体新药。海外方面由合作伙伴Summit主导的临床研究正在进行中。截至2025年10月依沃西已对13个癌种进行临床研究。
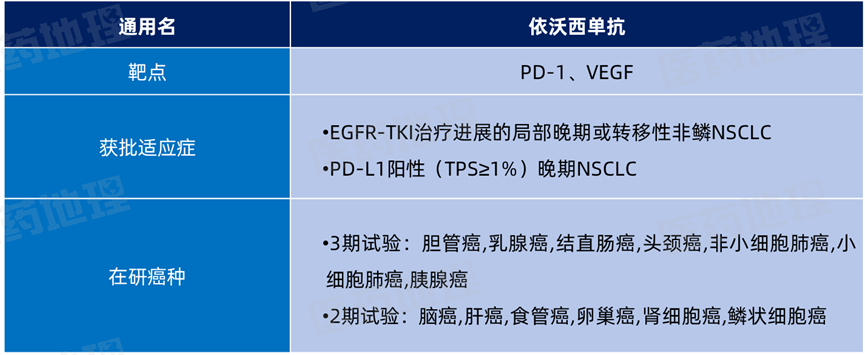
依沃西单抗全球研发进展
数据来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
TROP2 ADC ——芦康沙妥珠单抗
芦康沙妥珠单抗(sac-TMT)是科伦博泰拥有自主知识产权的新型TROP2抗体偶联药物(ADC)。10月19日,其针对EGFR突变非小细胞肺癌的III期临床研究——OptiTROP-Lung04的研究结果在ESMO年会主席论坛上重磅发布,并同步发表于《新英格兰医学杂志》(NEJM)。该研究旨在评估芦康沙妥珠单抗在既往接受EGFR-TKI治疗后疾病进展的EGFR突变晚期非小细胞肺癌患者中的疗效与安全性。研究结果显示,芦康沙妥珠单抗在EGFR-TKI耐药NSCLC治疗中,不仅显著延长PFS,更实现OS的显著延长,同时具备良好的安全性。
根据Pharma ONE药物研发大数据平台显示,芦康沙妥珠单抗已在中国获批三项适应症:三阴性乳腺癌、EGFR-TKI及含铂化疗后进展的EGFR突变非鳞NSCLC和EGFR-TKI治疗后进展的EGFR突变非鳞NSCLC,成为全球首个获批肺癌适应症的TROP2 ADC。海外方面由合作伙伴默沙东主导的临床研究正在进行中。截至2025年10月,芦康沙妥珠单抗已对8个癌种进行临床研究。
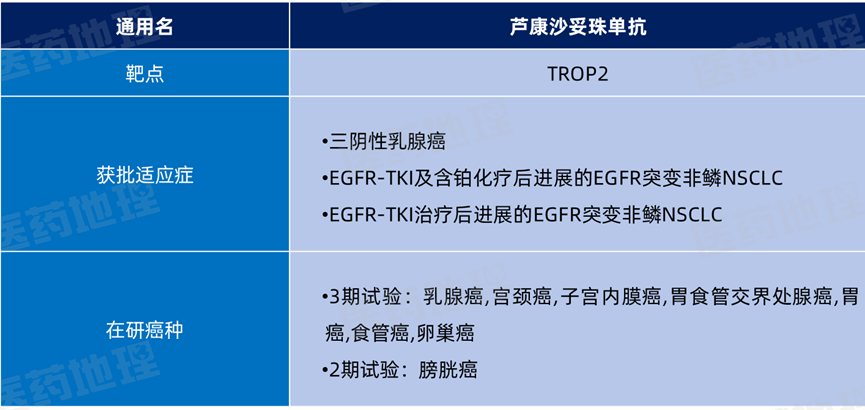
芦康沙妥珠单抗全球研发进展
数据来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
ADC+IO——维迪西妥单抗联合特瑞普利单抗
维迪西妥单抗是由荣昌生物研发的我国首个原创抗体偶联药物(ADC),也是我国首个同时获得美国FDA和中国国家药监局授予突破性疗法认定的ADC药物。2025年10月19日,其III期临床研究RC48-C016的结果在ESMO年会主席论坛上发布并同步发表于《新英格兰医学杂志》。该研究旨在评估维迪西妥单抗联合特瑞普利单抗,对比化疗,用于一线治疗HER2表达局部晚期或转移性尿路上皮癌的疗效与安全性。研究结果显示,RC48-C016研究已达到预设的无进展生存期(PFS)和总生存期(OS)双主要终点。经盲态独立影像评审委员会(BIRC)评估,联合治疗组的中位PFS为13.1个月,中位OS为31.5个月,相较于对照组,联合方案展现出显著的统计学优势和临床获益。
根据Pharma ONE药物研发大数据平台显示,维迪西妥单抗已在中国获批三项适应症:胃癌、尿路上皮癌和HER2阳性伴肝转移乳腺癌,是我国首个原创抗体偶联(ADC)药物。海外方面由合作伙伴辉瑞主导的临床研究正在进行中。截至2025年10月,维迪西妥单抗已对9个癌种进行临床研究。
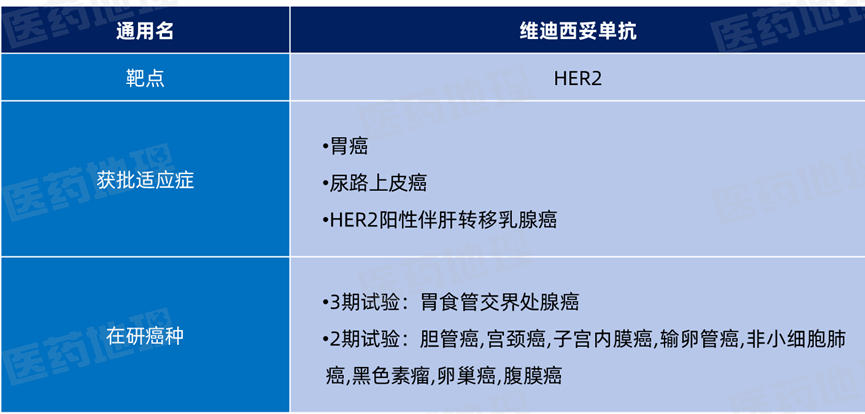
维迪西妥单抗全球研发进展
数据来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
结语
2025年ESMO年会无疑是中国创新药进程中的一座重要里程碑。依沃西、芦康沙妥珠单抗和维迪西妥单抗在三场主席研讨会上的联袂登场,不仅是中国研发实力的集中彰显,更标志着中国创新药实现了从国际舞台边缘到中心的跨越,正以“并跑者”乃至“领跑者”的姿态,在全球肿瘤治疗领域占据愈发关键的一席之地。

 切换平台
切换平台